新型コロナ経口薬「モルヌピラビル」の安全性
メルクの経口薬「モルヌピラビル」が特例承認されましたが、日本の政府もマスコミもその安全性についてほとんど言わないのが気になります。
テレ朝news(2021/12/25)コロナ飲み薬を国内初承認「切り札になり得る」

厚生労働省は24日、新型コロナウイルスの飲み薬「モルヌピラビル」を特例承認しました。コロナ向けに開発された飲み薬が承認されるのは国内初です。
後藤厚労大臣:「軽症者向けの経口治療薬は国民が安心して暮らせるための切り札になり得る」
本当にこの薬は切り札になるのでしょうか。
この薬の有効性と安全性はかなり微妙なようです。
メルクのコロナ経口薬にFDA使用許可-妊娠中は控えるよう警告
メルクが米リッジバック・バイオセラピューティクスと共同で開発したモルヌピラビルは、重症化リスクがある18歳以上の自宅療養者を対象とする。軽度から中等度の症状がある成人患者の入院および死亡のリスクが30%低下すると、試験結果で示された。
FDAは妊娠中のモルヌピラビル使用は避けるよう勧告しており、メルクは男性、女性とも服用中の性行為の際には避妊すべきだとしている。FDAの感染症部ディレクター、ジョン・ファーリー氏は記者団との電話会見で、モルヌピラビルに関しては「便益とリスクで難しい判断」を迫られたと説明。諮問委員会の会合が先月開かれたのはそのためだと述べた。ファイザー製についてはそのようなことはなかったと指摘した。
モルヌピラビルのラベルには、他の治療選択肢にアクセス不能の場合、あるいは臨床的に適切と判断された場合に使用すべきだと表示される。これが、ファイザー製のほうが望ましいとFDAは考えているのではないかとの疑念につながっている。FDAはメルク製よりファイザー製の使用を必ずしも推奨しているわけではないとしている。
この薬の新型コロナに対する入院と死亡の予防効果は、中間解析時は約50%でしたが、その後約30%に低下しています。
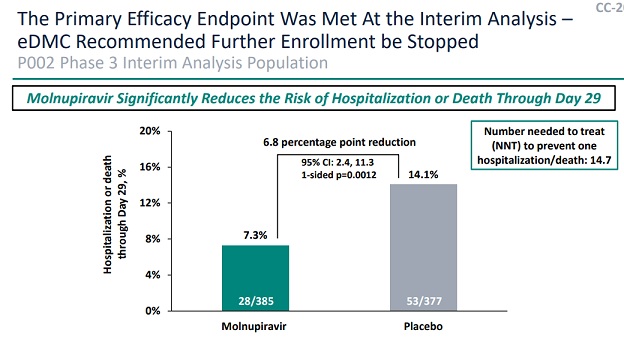
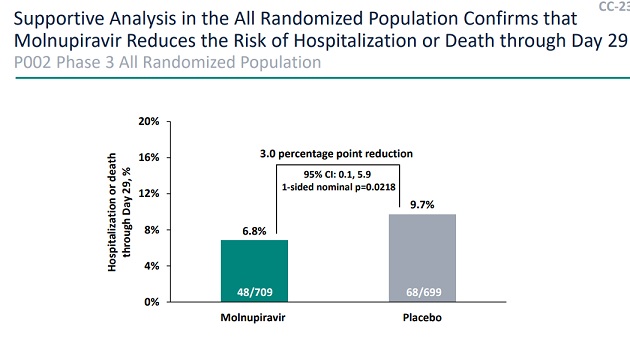
FDA Antimicrobial Drugs Advisory Committee Meeting (2021/11/30) Merck Presentations
フランスはこの治験結果があまり良くなかったことを理由に、注文をキャンセルしたそうです。
Bloomberg(2021/12/23)フランス、メルクのコロナ経口薬発注を取り消し-ファイザー製に変更
フランスのベラン保健相は22日、米製薬会社メルクが開発した新型コロナウイルス感染症の経口治療薬「モルヌピラビル」について、治験で期待通りの効果が得られなかったため、発注をキャンセルしたと明らかにした。米ファイザー製の経口薬「パクスロビド」の調達に切り替える。
効果が30%でも早く使えるならいいという考え方もありますが、この薬は副作用のリスクが大きな懸念だと思います。
以下はFDAのニュースリリースの抜粋です。
FDA NEWS RELEASE (2021/12/23)Coronavirus (COVID-19) Update: FDA Authorizes Additional Oral Antiviral for Treatment of COVID-19 in Certain Adults
FDAは、特定の成人のCOVID-19の治療のために追加の経口抗ウイルス薬を承認します
米国食品医薬品局は、SARS-CoV-2ウイルス検査の結果が陽性で重症化リスクが高く、FDAによって承認された代替の治療方法が困難な人のために、メルクのモルヌピラビルの緊急使用許可(EUA)を発行しました。モルヌピラビルは骨や軟骨の成長に影響を与える可能性があるため、18歳未満の患者への使用は許可されていません。
動物の生殖研究の結果に基づくと、モルヌピラビルは妊娠中の人に投与すると胎児に害を及ぼす可能性があります。したがって、モルヌピラビルは妊娠中の使用はお勧めしません。
出産の可能性のある女性は、モルヌピラビルによる治療中および最終投与後4日間、信頼できる避妊方法を正しく一貫して使用することをお勧めします。
出産の可能性のある女性と性的に活発な生殖能力のある男性は、モルヌピラビルによる治療中および最終投与後少なくとも3か月間、信頼できる避妊方法を正しく一貫して使用することをお勧めします。
これらの注意事項はモルヌピラビルの作用機序に起因することで、以前から指摘されていました。
モルヌピラビルは、ウイルスのRNAに突然変異を起こさせることによって、ウイルスの増殖を阻害します。
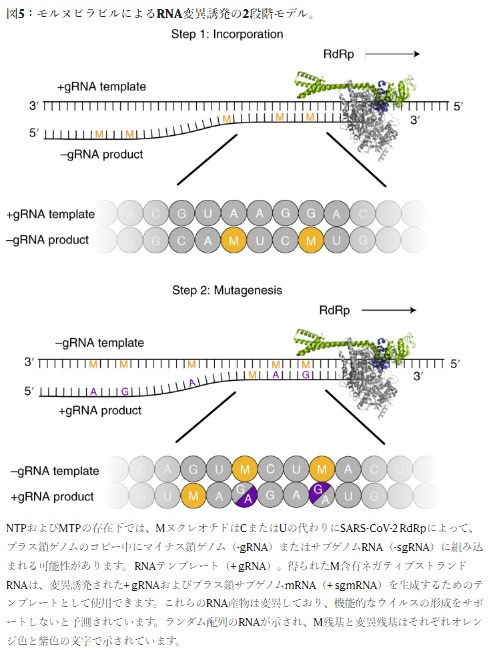
Mechanism of molnupiravir-induced SARS-CoV-2 mutagenesis
この突然変異がウイルスだけに作用すればいいのですが、人の細胞のDNAにも影響する可能性が指摘されています。
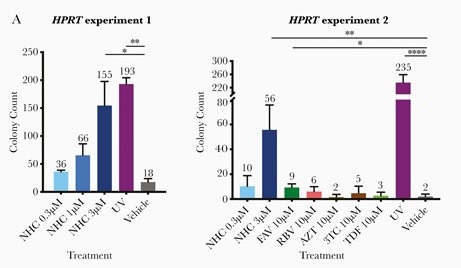
以下はモルヌピラビルの代謝物であるNHCの遺伝子毒性を比較したグラフです。
左のグラフは、NHCの濃度を変えた時の遺伝子毒性を比較したもの。
右のグラフは、NHCと他の抗ウイルス薬の遺伝子毒性を比較したもの。
(3TC:ラミブジン, AZT:ジドブジン, FAV:ファビピラビル, RBV:リバビリン)
このグラフを素直に見ると、NHC(モルヌピラビル)はFAV(ファビピラビル[アビガン])よりずっと遺伝子毒性が高くなっています。
PHARMACEUTICAL TECHNOLOGY (2021/11/3)Molnupiravir: long-term safety questions linger as approvals approach
モルヌピラビルの安全性に関する懸念
Covid-19に対するモルヌピラビルのメカニズムには、ヒト細胞における変異原性の可能性について懸念する専門家がいます。
この薬はウイルスRNAのみを破壊することを目的としていますが、ヒトDNAに組み込まれ、突然変異を引き起こす可能性もあります。
宿主DNAの突然変異は、「癌の発生に寄与するか、発生中の胎児または精子前駆細胞への取り込みを通じて先天性欠損症を引き起こす可能性がある」と述べています。ノースカロライナ大学の生化学および生物物理学部のロン・スワンストロム教授も、この薬の安全性について懸念を抱いています。モルヌピラビルは「潜在的に重要な抗ウイルス戦略」ですが、この化合物の長期的な影響が人間にどのような影響を与えるかを知ることは不可能です。
FDAもかなり限定した使い方をしようとしていますが、リスクと有効性を考えると、このモルヌピラビルは誰でも積極的に使う薬ではなさそうです。
いずれにせよ、現時点ではどう考えても、モルヌピラビルよりファイザーの「パクスロビド」の方が有効性も安全性も上だと思います。
FDAはすでにパクスロビドの緊急使用許可を出しているので、厚労省も申請が出されたらすぐ承認するはずです。
日本の政府とマスコミは、ほとんどリスクを言わずにいい事ばかり報道していますが、メルクへの忖度でしょうか?
騙されないようにしたいものです。